Casi el 30% de la población española sufre alteraciones en el metabolismo de la glucosa, lo que puede acarrear graves problemas de salud y complicaciones como la diabetes. “La diabetes es un mal silencioso. A menudo no damos mucha importancia a tener la glucosa alta, ya que no produce ningún síntoma. Pero sus efectos se acumulan durante mucho tiempo y aumentan el riesgo de padecer enfermedades cardiovasculares graves como infartos de miocardio o ictus, y otros como pérdida de la visión por afectación de la retina, daños en los nervios y extremidades, o insuficiencia renal que puede acabar en diálisis y trasplante de riñón”, explica Joan-Marc Servitja, investigador del grupo IDIBAPS Patogenia y prevención de la diabetes, dirigido por Anna Novials.
Los datos indican que en España cuatro millones y medio de personas sufren diabetes, es decir, casi un 14% de la población. “Sin embargo, la mitad no lo saben. Es lo que conocemos como la diabetes desconocida”, señala Novials. “A pesar de la relevancia de estas cifras, el dinero destinado a la investigación es inferior al que reciben otras enfermedades como el cáncer, el Alzheimer, el Parkinson o la obesidad, aunque todas ellas tienen una estrecha relación con la diabetes. Esto nos preocupa a los investigadores, que luchamos por visibilizar la enfermedad y por educar a la sociedad sobre su importancia”.
Un nombre, varias enfermedades
La palabra diabetes no se refiere a una única enfermedad, sino que engloba varios trastornos.
La diabetes tipo 1 es una enfermedad autoinmunitaria que se caracteriza por un aumento de los niveles de glucosa en sangre, porque el propio sistema inmunológico del organismo ataca y destruye las células del páncreas que generan la insulina.
La diabetes tipo 2 también se caracteriza por un aumento de la concentración de glucosa en sangre. En este caso, la causa es la incapacidad del cuerpo para producir o poder utilizar de manera adecuada la propia insulina. Se inicia en adultos, de ahí el nombre popular de diabetes de la gente mayor. Este tipo de diabetes se asocia a la obesidad y el sedentarismo.
"El 90% de los casos de diabetes son de tipo 2. La diabetes de tipo 1 es la segunda más importante en prevalencia, pero también cabe destacar la diabetes gestacional y las diabetes monogénicas o de causa genética", comenta Servitja. “De hecho, cada vez se vigila más la diabetes gestacional, puesto que es una especie de preaviso. Si a lo largo de los años la madre ha sufrido sobrepeso u obesidad, aumentan sus posibilidades de padecer diabetes tipo 2”.
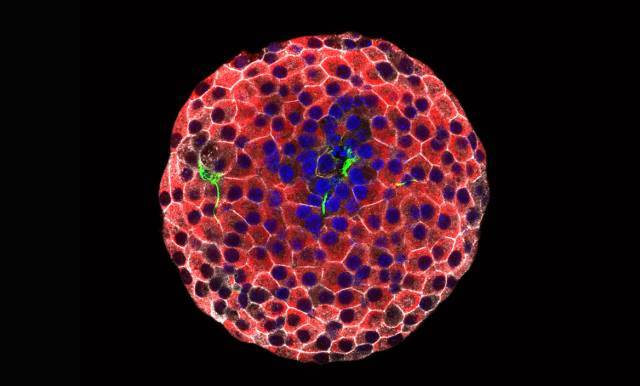
Imagen de inmunofluorescencia de un islote pancreático. Se observan células beta íntegras (rojo), células beta destruidas (verde) y sus núcleos (azul). [Júlia Rodríguez]
¿Es posible restaurar la producción de insulina?
La investigación en diabetes tipo 1 se centra, principalmente, en averiguar por qué el sistema inmunitario reacciona contra las células beta del páncreas y en cómo detener este ataque, así como en desarrollar terapias celulares que permitan obtener células beta funcionales para trasplantarlas a los pacientes. La diabetes tipo 2 es una enfermedad multifactorial, que requiere abordar desde la genética a los mecanismos metabólicos y de inflamación para obtener la imagen completa y entender lo que ocurre. Además, la dieta y el estilo de vida también juegan un importante papel en el desarrollo de la enfermedad. Por esta razón, se trabaja en líneas de prevención y educación de la población.
Actualmente, no disponemos de una cura eficaz para la diabetes. "La administración de insulina permite cronificar la diabetes, vivir con la enfermedad, pero no restaura la función del páncreas, solo la sustituye", puntualiza Rosa Gasa, investigadora del grupo IDIBAPS Investigación traslacional en diabetes, lípidos y obesidad, liderado por Josep Vidal.
Tanto en la diabetes tipo 1 como en la tipo 2 la producción de insulina se altera. Sin embargo, en la primera, se observa una insuficiencia de insulina desde el inicio de la enfermedad, mientras que en los primeros estadios de la segunda hay un exceso, que finalmente se vuelve en déficit. “Esto se explica por lo que ocurre en las células beta del páncreas en cada uno de estos dos tipos de diabetes”, comenta Gasa. “Las células beta, localizadas en los islotes pancreáticos, son las encargadas de producir y secretar la insulina. En la diabetes tipo 1, la reacción autoinmunitaria destruye casi totalmente estas células. Por el contrario, en la diabetes tipo 2, las células beta producen insulina, pero los tejidos se vuelven resistentes y no responden a la hormona. Esto provoca que el islote pancreático aumente su secreción. Sin embargo, a la larga, dicho sobreesfuerzo causa la disfunción del tejido”.
El equipo de Vidal y Gasa investiga cómo regenerar las células beta pancreáticas. En concreto, busca factores que permitan expandir las pocas células que quedan. “Incluso en páncreas de pacientes con diabetes tipo 1 analizados post-mortem se han encontrado células beta. Esto nos indica que de alguna forma, a pesar de su destrucción, el tejido intenta regenerarse”. La expansión de las células beta se produce durante el primer año de vida en los humanos y durante el período de lactancia en los ratones. El estudio de este período neonatal en roedores ha permitido al grupo Vidal-Gasa identificar una proteína secretada por el tejido óseo, el factor Wisp1, que podría ser clave para el desarrollo del páncreas. “Esta molécula también aumenta en niños y disminuye en personas adultas, cuando se detiene el crecimiento del esqueleto. Es probable que existan otros factores que también participan en la expansión de las células beta. Encontrarlos puede suponer un importante avance en la regeneración del tejido pancreático que queda”.
En paralelo, el equipo de Vidal y Gasa trabaja en una línea de investigación encaminada a la creación de células beta a partir de células de la piel. “El proceso consiste en tomar células diferenciadas, como los fibroblastos que hay en la dermis y reprogramarlas de forma directa para que expresen los genes de otro tipo celular diferente”, explica Gasa. “Hoy en día, sólo introduciendo cinco factores de transcripción, unas proteínas que se unen al ADN y regulan la expresión de los genes, podemos reprogramar fibroblastos para que produzcan y liberen insulina humana en respuesta al aumento de glucosa en sangre”. En ratones, esta secreción de insulina se observa hasta 30 días después del trasplante. "Esto nos indica que durante todo este período, la reprogramación se mantiene y las células no mueren".
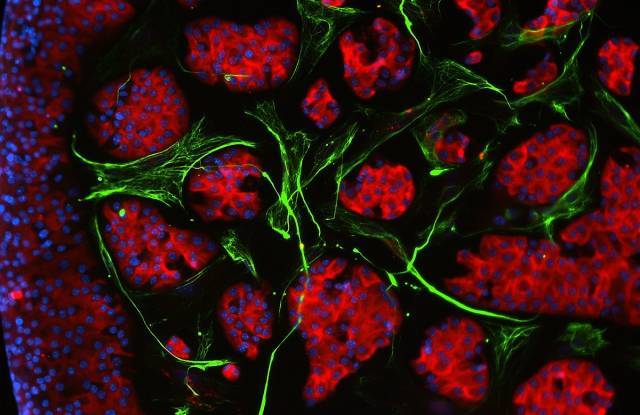
Imagen de inmunofluorescencia de células de islotes pancreáticos en cultivo (rojo), rodeadas de fibroblastos (verde). Los núcleos celulares se observan teñidos de azul. [Juan Moreno]
La ventaja de este método es que podemos realizar trasplantes a partir de una muestra muy pequeña de piel del mismo individuo, hecho que reduce el riesgo de rechazo. “Trasplantar un páncreas entero es una operación muy compleja, que se realiza solo cuando no existe otra alternativa. Otra opción es la implantación de islotes pancreáticos de donantes. El problema es que el proceso de aislamiento se realiza post-mortem, es muy poco eficiente y para cada paciente se necesitan entre dos y tres donantes. Además, es necesario administrar un tratamiento con inmuno-supresores de por vida. Por último, en casos de diabetes tipo 1, aunque durante el primer año el 80% de los trasplantados puede prescindir de las inyecciones de insulina, a los cinco años gran parte de las células implantadas han muerto y se requiere un nuevo trasplante. Así que no es un cuidado viable a largo plazo”, expone la investigadora.
Proteger las células beta
Joan-Marc Servitja coincide en destacar el potencial terapéutico de los trasplantes. "Sin embargo, la cuestión es que si no conseguimos frenar la destrucción de las células nos encontraremos de nuevo ante un tratamiento que cronifica la enfermedad, pero que no la cura, puesto que constantemente deberemos reponerlas". Para proteger las células beta, el equipo de Novials y Servitja ha evaluado el uso de moléculas con propiedades antiinflamatorias, como la alfa-1 antitripsina. “Es uno de los pocos proyectos que tenemos en diabetes tipo 1, ya que nuestra investigación se centra en la diabetes tipo 2, pero obtuvimos resultados prometedores. Estos compuestos inhiben la acción de las citoquinas secretadas por el sistema inmunitario y, por tanto, el ataque contra las células beta. Además, causan muy pocos efectos secundarios”.
"Esperamos avanzar estos estudios en pacientes", declara Novials. “Sin embargo, a menudo intervenimos en etapas muy tardías de la enfermedad, hecho que dificulta la protección y regeneración del páncreas. Por esta razón, una de nuestras principales líneas de investigación son los biomarcadores. Moléculas que nos permitan detectar personas prediabéticas. De hecho, hemos identificado pequeñas moléculas de ARN, o micro-ARNs, específicas, en una población con niveles ligeramente elevados de glucosa en sangre, pero que todavía no ha desarrollado diabetes tipo 2”.
El estudio de estos micro-ARNs, que circulan por la sangre dentro de unas vesículas llamadas exosomas, pone de relieve otro aspecto de la diabetes: su complejidad. Aunque el páncreas centra buena parte de la investigación, lo cierto es que en el desarrollo de la enfermedad intervienen otros órganos y tejidos, como el hígado, el músculo, el tejido adiposo o el cerebro. La comunicación entre ellos podría explicar el trastorno metabólico que caracteriza a la diabetes. "El páncreas y el cerebro tienen mucho en común", señala Servitja. “En la diabetes tipo 2, se forman depósitos de un péptido, llamado amilina, en el tejido pancreático. Es un proceso muy parecido al que ocurre en la enfermedad de Alzheimer, donde los agregados del péptido amiloide beta se acumulan en las neuronas y ocasionan su muerte”, continúa Novials. La diabetes y el Alzheimer también comparten una posible diana terapéutica, la proteína BACE2, como han demostrado los investigadores en un artículo recientemente publicado.

Imagen obtenida por microscopía electrónica de exosomas, vesículas extracelulares que contienen proteínas, así como moléculas de ADN y ARN, y las transportan por el torrente sanguíneo. [Vicent Ribas]
En condiciones no patológicas, la amilina se secreta conjuntamente con la insulina, pero por razones que todavía se desconocen, se pliega mal y se acumula, lo que provoca la destrucción de las células beta. “Nuestro modelo de diabetes tipo 2 son ratones que sobreexpresan la amilina. Además, los engordamos para que sus características sean más parecidas a las de los pacientes. Gracias a este modelo hemos hallado dianas terapéuticas para recuperar la función de las células beta”, dice Servitja.
Otra línea de intervención que permite mejorar la diabetes es el ejercicio. “El estilo de vida es muy importante. En el caso de la diabetes tipo 2, nuestro grupo ha observado que el ejercicio mejora el metabolismo y normaliza los niveles de micro-ARN que contribuyen al estrés del páncreas. Sin embargo, es necesario informar a los pacientes sobre la pauta que más les conviene según su enfermedad. Por ejemplo, en personas con diabetes tipo 1, sesiones largas y prolongadas de ejercicio pueden provocar hipoglucemias, bajadas de glucosa considerables. En cambio, hemos demostrado que entrenamientos interválicos, cortos y de alta intensidad como el HITT, conllevan un menor riesgo de provocar hipoglucemias”, puntualiza Novials.
“Lo más probable es que la cura de la diabetes requiera el uso de la medicina personalizada, adaptada a cada paciente, y las terapias combinadas, que protejan a la vez que regeneren el tejido. Y para conseguir este objetivo, la investigación multidisciplinar, donde participen investigadores de diferentes campos, es esencial”, concluye Gasa.
Este contenido se ha elaborado gracias al apoyo de la Fundación Española para la Ciencia y la Tecnología (FECYT).




