Un equip de la Universitat de Barcelona (UB) i de l’Institut d’Investigacions Biomèdiques August Pi i Sunyer (IDIBAPS) ha identificat un mecanisme implicat en el moviment del colesterol dins de les cèl·lules. La recerca, publicada al Journal of Cell Biology, mostra com la proteïna SNX13 té un paper clau a l’hora de transportar aquest lípid fora dels lisosomes, els orgànuls encarregats de la digestió cel·lular. Aquests resultats podrien tenir implicacions en el futur desenvolupament de tractaments contra patologies causades per disfuncions en el transport del colesterol intracel·lular, com ara la malaltia de Niemann-Pick de tipus C.
A la recerca hi participen els investigadors de la UB i de l’IDIBAPS Albert Lu, primer autor de l’article, i Carles Enrich, cap del grup Endocitosi i tràfic intracel·lular de proteïnes i colesterol, juntament amb investigadors de la Universitat de Stanford.
Els efectes nocius del desequilibri en els nivells de colesterol
La major part del colesterol que les cèl·lules utilitzen prové del seu exterior i arriba als lisosomes, en què es distribueix a diferents compartiments intracel·lulars. No obstant això, encara hi ha moltes preguntes pendents relacionades amb els esdeveniments moleculars precisos que regulen la sortida del colesterol d’aquest orgànul i el seu posterior transport cap a la membrana i el reticle endoplasmàtic de les cèl·lules. L’objectiu d’aquesta recerca ha estat estudiar el mecanisme gràcies al qual el colesterol surt dels lisosomes. “Aquest procés requereix l’acció coordinada dels transportadors NPC1 i NPC2, que juntament amb el lípid lisosòmic bis-(monoacilglicerol)-fosfat (BMP) mobilitzen i exporten el colesterol lliure”, explica Enrich.
La regulació del tràfic intracel·lular de colesterol i de la quantitat que en reben els diferents orgànuls cel·lulars és molt important per a l’equilibri —o homeòstasi— del colesterol dins la cèl·lula. Errors o disfuncions en el seu transport provoquen un desajustament que causa trastorns com ara la malaltia de Niemann-Pick de tipus C. Es tracta d’una malaltia, actualment sense cura, produïda per mutacions en els transportadors de colesterol lisosòmics NPC1 i NPC2. Això impedeix metabolitzar el colesterol i altres greixos amb normalitat, la qual cosa afecta greument el fetge, la melsa i el cervell.
Cribratge genètic de tipus CRISPR/Cas9 en tot el genoma
Per tal d’identificar reguladors de l’equilibri del colesterol, els investigadors van fer cribratges genètics de tipus CRISPR/Cas9 en tot el genoma. Aquesta metodologia permet interrogar, de manera massiva i paral·lela, tot el genoma humà respecte a un procés biològic concret, procediment que genera una gran quantitat de dades. En aquest estudi, el cribratge es va aplicar en condicions normals, però també bloquejant la proteïna NPC1, amb el propòsit d’identificar els components cel·lulars que poden exportar el colesterol de manera paral·lela a aquest transportador.
Aquesta estratègia va permetre descobrir gens que, quan s’eliminen, alteren els nivells intracel·lulars del colesterol o del BMP. ”Els nostres cribratges genètics van identificar un elevat nombre de gens implicats en la regulació metabòlica del colesterol i el BMP, el paper dels quals no es coneixia en aquest context. A més, vam confirmar una estreta correlació i regulació entre els nivells d’aquests dos lípids”, destaca Lu.
Una de les molècules implicades en aquest procés és l’SNX13, una proteïna del reticle endoplasmàtic que regula negativament la sortida del colesterol dels lisosomes cap a la membrana plasmàtica i, així, fa disminuir la quantitat d’aquest lípid. “En absència de la funció de l’NPC1, la reducció de l’SNX13 va provocar una redistribució del colesterol lisosòmic cap a la membrana plasmàtica, la qual cosa indica que l’SNX13 podria ser un regulador important en aquesta via de transport del colesterol”, explica Lu.
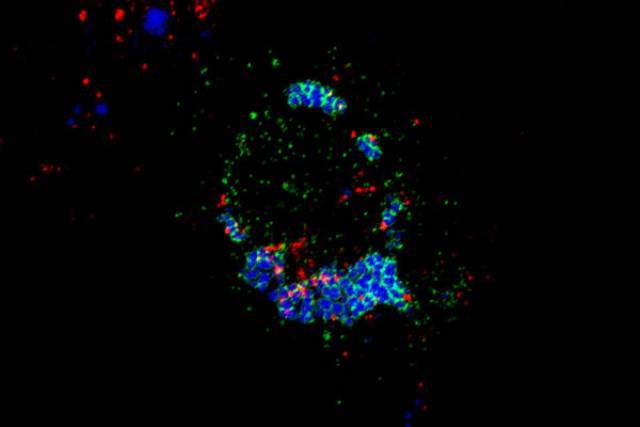
Imatge de microscòpia confocal en què es poden observar la proteïna SNX13 (color verd) en regions del reticle endoplasmàtic que estableixen contactes amb gotes lipídiques (color blau) i lisosomes en què està present el lípid BMP (color vermell).
Una visió inesperada dels mecanismes de regulació
Aquests resultats proporcionen una visió inesperada de la regulació d’aquests lípids, ja que hi ha pocs mecanismes alternatius —i en la major part dels casos són desconeguts— que permetin la sortida del colesterol quan el transportador NPC1 està inhibit o ha mutat. “Nosaltres ja vam descriure fa poc una via alternativa regulada per l’annexina A6, i amb aquest nou treball aportem noves evidències que indiquen que paral·lelament a l’NPC1 pot haver-hi rutes alternatives de sortida del colesterol lisosòmic”, subratlla Enrich.
El descobriment de molècules capaces de revertir els efectes causats per la disfunció de l’NPC1, com és el cas de l’SNX13, podria suposar l’existència de “futures dianes terapèutiques en el tractament de la malaltia de Niemann-Pick de tipus C, ja que un millor coneixement de les molècules que participen en el contacte entre orgànuls pot permetre la manipulació del transport de lípids i ions, així com restablir l’homeòstasi cel·lular”, conclouen els investigadors.
Article de referència:
Lu, A.; Hsieh, F.; Sharma, B. R.; Vaughn, S. R.; Enrich, C.; i Pfeffer S. R. CRISPR screens for lipid regulators reveal a role for ER-bound SNX13 in lysosomal cholesterol export. Journal of Cell Biology, desembre de 2021. Doi: https://doi.org/10.1083/jcb.202105060




